【ポイント】
① 亜鉛は生体必須微量ミネラルですが、その制御破綻がどのような分子メカニズムで細胞毒性につながるのかはほとんど不明でした。
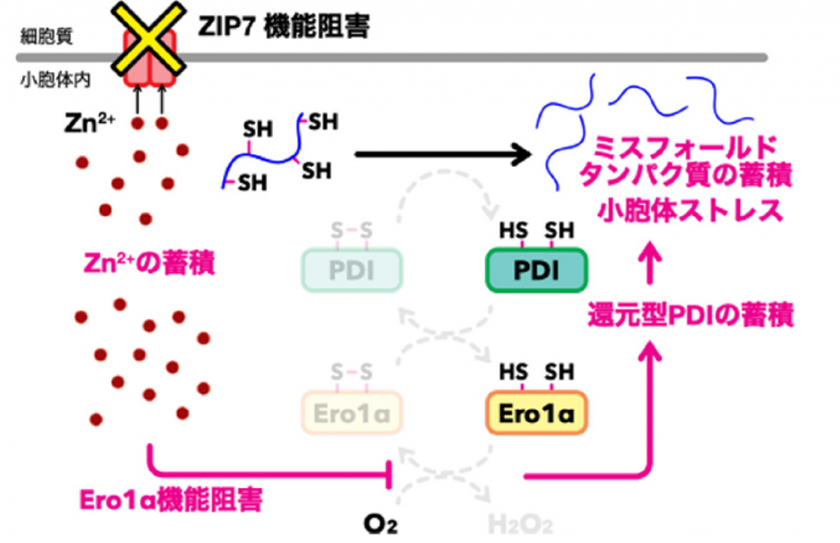
② 本研究で、小胞体(※1)に存在する亜鉛トランスポーター(※2)ZIP7を阻害すると、小胞体中に亜鉛イオンが劇的に蓄積することを発見しました。
この過剰亜鉛が小胞体内酸化酵素の機能を阻害し、その結果、NotchやEGF受容体といった細胞増殖や癌発生に重要な働きを持つ膜タンパク質のジスルフィド結合形成(※3)を伴う生合成が阻害されることを突き止めました。
③ 亜鉛イオン自体は2価で安定な金属イオンであるため酸化還元活性を持ちませんが、酸化酵素の働きを調節することで小胞体の酸化還元(レドックス)制御に重要であることを明らかにしました。
今後の研究が進むことで、亜鉛の制御破綻による病態発生のメカニズムを、亜鉛とレドックスのクロストークの観点から解明できることが期待されます。
——————————
【概要】
亜鉛は必須微量元素の一つで、様々なタンパク質と結合・解離し多様な生命現象を支えています。そのため、亜鉛の不足や過剰は免疫機能、創傷治癒、味覚嗅覚障害といった病態を引き起こします。
細胞膜や細胞内小器官(オルガネラ)の膜上で亜鉛トランスポータータンパク質が生体膜を隔てた亜鉛輸送を行うことで、細胞内の亜鉛濃度調節がなされています。
ヒトには10種類のZnT、14種類のZIP亜鉛トランスポーター遺伝子がそれぞれ発見されており、それらの欠損が遺伝性疾患と関連することが多く報告されています。
しかしながら、亜鉛イオン濃度制御の破綻が細胞機能の破綻につながる詳細な分子機構はほとんど未解明でした。
九州大学生体防御医学研究所の天貝佑太助教、渡部聡准教授、稲葉謙次主幹教授(未来社会デザイン統括本部、医療・健康ユニット/高深度オミクスグループメンバー)らの研究グループは、新潟大学の松本雅記教授、東北大学多元物質科学研究所の水上進教授、小和田俊行准教授、京都先端科学大学の寳関淳教授、およびサン・ラファエル研究所(イタリア)のロベルト シティア教授らと共同で、ZIP7の機能阻害が小胞体中の亜鉛イオン濃度を定常状態の1,000,000倍まで増加させることを発見し、この亜鉛が小胞体酸化酵素Ero1αを直接阻害することを解明しました。
その結果、小胞体が本来の酸化的な環境から還元的な環境に変化し、生体内の重要な膜タンパク質であるNotchやEGF受容体のジスルフィド結合形成が阻害され、正しい立体構造が形成されなくなることを解明しました。
今回の成果は、小胞体中の亜鉛制御破綻がレドックス制御破綻につながることで細胞毒性を生み出す具体的な分子機構を解明したものになります。
本研究成果をもとに、亜鉛制御異常が引き起こす病態発生メカニズムが解明されていくものと期待されます。
本研究成果は英国の国際誌「Nature Communications」に2026年4月22日(水曜日)(日本時間)に掲載されました。
詳細は、こちらをご確認ください。
——————————
【用語解説】
(※1)小胞体
説明 細胞内小器官の一つ。細胞中で新規に合成された分泌タンパク質や膜タンパク質は小胞体中に挿入される。これらのタンパク質は正しいシステイン残基間でジスルフィド結合が形成されることで天然型の立体構造を獲得するため、小胞体内にはジスルフィド結合形成を促す一連のレドックス酵素が備えられている。
(※2)亜鉛トランスポーター
説明 生体膜を隔てて亜鉛イオンの輸送を行う膜内在性のタンパク質。細胞外やオルガネラ内腔から細胞質方向へ亜鉛イオンを輸送するZIPファミリー、その反対方向へ輸送するZnTファミリーの2種類が知られる。
(※3) ジスルフィド結合
説明 近接する二つのシステインと呼ばれるアミノ酸残基の硫黄原子間で、酸化反応より形成される共有結合。タンパク質の立体構造形成や活性の調節に寄与する。
(※4) ミスフォールドタンパク質
説明 正しい立体構造を形成できず、構造や機能が異常な状態で細胞内に存在するタンパク質。これが過剰に蓄積すると、細胞ストレスを引き起こし、細胞死に至ることもある。